Vom Zyklusmonitoring zur Spermien-Mikroinjektion

Mit dem 20. Geburtstag des ersten "Retortenbabys" Louise Brown, geboren am 25.07.1978, sind die Verfahren der assistierten Reproduktion erneut in den Mittelpunkt des öffentlichen Interesses gerückt.
Ging es damals ausschließlich darum, Frauen mit definitiven Passagestörungen der Eileiter mit Hilfe der In-vitro-Fertilisation (IVF) zu einem eigenen Baby zu verhelfen, so hat sich die Indikationsstellung in den letzten Jahren auch auf die Formen der andrologischen Subfertilität bis hin
zur Azoospermie ausgedehnt.
Methoden der assistierten Reproduktion
Bis Anfang der 90‘er Jahre umfasste das Behandlungsspektrum der Reproduktionsmedizin das Zyklusmonitoring, die Zyklusoptimierung, das Anfertigen von Spermiogrammen, die intrauterine Insemination, die GIFT-Behandlung und die In-vitro-Fertilisation (IVF).
1993 kamen in Deutschland die intrazytoplasmatische Spermieninjektion (ICSI) einschließlich mikrochirurgischer epididymaler Spermienaspiration (MESA) und testikulärer Spermienextraktion (TESE) in Verbindung mit der Kryokonservierung von Spermien und befruchteten Eizellen im Vorkernstadium dazu. Erst mit der ICSI konnte sich eine viel versprechende Alternative zur herkömmlichen IVF bei erheblicher andrologischer Subfertilität entwickeln. Im Vergleich zu anderen Techniken der assistierten Fertilisation, wie Zonadrilling (ZD), partieller Zonadissektion (PZD) oder subzonaler Insemination (SUZI) ist die ICSI zur Zeit die erfolgreichste Behandlungsmethode.
Dennoch sollte die andrologische Subfertilität aber nur dann als Indikation für ICSI dienen, wenn entweder Spermiendichten von unter 3 - 5 Mio./ml vorliegen bzw. nicht davon ausgegangen werden kann, dass für die IVF mindestens 200.000 progressiv mobile, gereinigte Spermien pro Eizelle zur Verfügung stehen, oder es bei 1 - 2 vorausgegangenen klassischen IVF-Versuchen bei ausreichender Oozytenanzahl nicht zu Fertilisationen kam. Weiterhin bestehen bei der MESA und der TESE die besten Chancen auf Erfolg, wenn sich die intrazytoplasmatische Spermieninjektion dem anschließt.
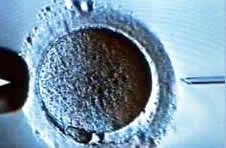
Durchführung der IVF und ICSI
Für die klassische IVF und die ICSI erfolgt die ovarielle Stimulation meistens im Rahmen des langen Protokolls. Hierbei erhalten die Patientinnen ab dem 20. Zyklustag im Vorzyklus täglich subcutan bzw. nasal ein GnRH-Analogon oder eine einmalige Injektion eines Depotpräparates.
Reife Metaphase-II-Oozyte vor der ICSI
2 Wochen nach Spritzenanfang und nach der Regelblutung beginnt die eigentliche ovarielle Stimulation. Stimuliert wird mit HMG, FSH oder rekombinantem FSH, in der Regel mit 150 IE täglich. Die HCG-Applikation (10.000 IE) erfolgt bei einem Durchmesser der Führungsfollikel ab 20 mm 36 Stunden vor der ultraschallgesteuerten vaginalen Follikelpunktion.
Im Anschluß an die vaginale Follikelpunktion kommen die gewonnenen Oozyten in ein mit 5% CO2 bei 37°C begastes Ham’s F10-Medium, um bei dem klassischen IVF-Verfahren nach ca. 4 - 5 Stunden mit einer genau festgelegten Menge an progressiv mobilen Spermien gemischt zu werden. Bei der ICSI-Variante erfolgt nach etwa 3 Stunden die Freipräparation der Eizellen.
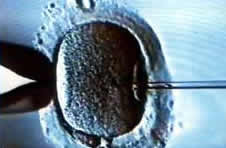
Injektion des Spermatozoons - an der Zona pellucida in der Injektionspipette zu sehen -
in das Ooplasma
Dazu müssen die Eizellen etwa 30 Sekunden lang in Hepes-gepuffertem Ham’s F10-Medium mit 80 IE Hyaluronidase gespült und mit Hilfe feinster Pipetten von der Cumulusmasse befreit werden.
Anschließend findet die Spermien-Mikroinjektion der reifen Metaphase-II-Oozyten statt.

Für die IVF und die ICSI erfolgt die Spermienaufbereitung durch Waschen in Ham’s F10-Medium, 10-minütiger Zentrifugation bei 500 G und anschließendes swim up (soweit möglich).
Bei der ICSI werden unter einem speziellen Mikroskop, das mit Manipulatoren für die Mikroinjektion ausgerüstet ist, die Oozyten mit der Haltepipette so gefasst, dass das Polkörperchen bei 6 Uhr zu liegen kommt.
Zwei befruchtete Eizellen mit jeweils zwei Pronuclei
Mit der Injektionspipette wird dann jeweils ein immobilisiertes Spermatozoon bei 3 Uhr in die Eizelle injiziert . Anschließend erfolgt die erneute Umsetzung der Eizellen in den Inkubator.

16 bis 18 Stunden nach dem Zusammenbringen von Oozyten und Spermien werden die Eizellen auf Fertilisationszeichen
(2 Pronuclei) hin untersucht und nach weiteren
26 bis 28 Stunden erfolgt der Embryotransfer.
Insgesamt werden bis zu 3 Embryonen
Ein Embryo - Zweizeller -
zwei Tage nach IVF bzw. ICSI
(Embryo - Zweizeller - zwei Tage nach IVF bzw. ICSI) mittels eines speziellen Embryotransferkatheters transzervikal in das Cavum uteri gebracht. Zur Unterstützung der lutealen Phase erhalten die Patientinnen 3mal täglich über 2 Wochen 200 mg Progesteron intravaginal und, vorausgesetzt es bieten sich keine Zeichen einer Überstimulation, zusätzlich am Transfertag 5.000 IE HCG i.m.
Ergebnisse
Schwangerschaftsraten in Abhängigkeit von den einzelnen Behandlungsmethoden an der Frauenklinik der Ev. Diakonissenanstalt (Bremer Zentrum für Fortpflanzungsmedizin)
Anzahl der behandelten Patientinnen
Anzahl der Zyklen (gesamt)
Spontanzyklen
Homologe intrauterine Insemination
IVF-Zyklen
ICSI-Zyklen
Abbruch des Beandlungszyklus
Spontan-Schwangerschaftsrate
Inseminations-Schwangerschaftsrate
IVF-Schwangerschaftsrate pro Embryotransfer
ICSI-Schwangerschaftsrate pro Embryotransfer
1996
316
507
20
139
175
173
22
27,8 %
14,7 %
18,9 %
30,5 %
1997
451
640
26
206
152
225
31
15,4 %
17,0 %
23,8 %
30,2 %
Mögliche Risiken
Im Hinblick auf mögliche Risiken kommt es bei dem ICSI-Verfahren zu einer normalen Embryonalentwicklung, Schwangerschaft und Geburt eines gesunden Kindes. So konnte die Brüsseler Arbeitsgruppe um van Steirteghem bei 1.180 Kindern, die nach ICSI geboren wurden (Stand 16.04.96), eine Fehlbildungsrate von 2,5% gegenüber einer Rate von 4 - 5% in der Normalpopulation nachweisen. Nur das Risiko für eine Chromosomenanomalie soll aufgrund der Selektion der andrologischen Ursachen für die Sterilität leicht erhöht sein. Daher empfehlen wir unseren Kinderwunsch-Paaren vor Behandlungsbeginn eine humangenetische Abklärung evtl. mit Karyotypisierung durchführen zu lassen. Die anderen Risiken wie Überstimulationssyndrom und Mehrlingsgravidität sind identisch denen der klassischen IVF-Behandlung. Hinsichtlich der Erfolgsaussichten ist die Schwangerschaftswahrscheinlichkeit bei einem Transfer von 3 Embryonen (mehr sind laut deutschem Embryonenschutzgesetz nicht erlaubt) rund 30%. Nach insgesamt 6 Behandlungszyklen und jeweils einem Transfer von 3 Embryonen steigt die sogenannte kumulative Schwangerschaftsrate auf 70%. Ist aber nach 6 Behandlungen keine Schwangerschaft eingetreten, nimmt statistisch gesehen bei weiteren Versuchen die Wahrscheinlichkeit auf eine Schwangerschaft nicht mehr zu sondern ab.
Fazit
In den letzten 20 Jahren sind weltweit weit über 200.000 IVF-Kinder geboren. Die Fortpflanzungsmedizin hat heute einen Entwicklungstand erreicht, der es ermöglicht, vielen Paaren den Wunsch auf ein eigenes Kind zu erfüllen, die selbst zur Zeit der Geburt von Louise Brown noch nicht darauf hätten hoffen können.
aus "Bremer Ärztejournal" Heft 10/98 © O. Drost, E.H. Schmidt
Literatur erhältlich bei den Verfassern Bremer Zentrum für Fortpflanzungsmedizin
Prof. Dr. med. Ernst Heinrich Schmidt und
Dr. med. Olaf Drost
Frauenklinik, Evang. Diakoniekrankenhaus
gGmbH Bremen
Gröpelinger Heerstraße 406 / 408
28239 Bremen
Tel. (0421) 61 02-0, Fax (0421) 61 02-12 29.
